薬物治療の標的分子を解明し、病気の治癒やQOLの改善を目指します。
分子薬物治療学研究室
論文業績の説明
Fujita K, Sugiura T, Okumura H, Umeda S, Nakamichi N, Watanabe Y, Suzuki H, Sunakawa Y, Shimada K, Kawara K, Sasaki Y and Kato Y. Direct inhibition and down-regulation by uremic plasma components of hepatic uptake transporter for SN-38, an active metabolite of irinotecan, in humans. Pharm Res 31: 204-215,2014.
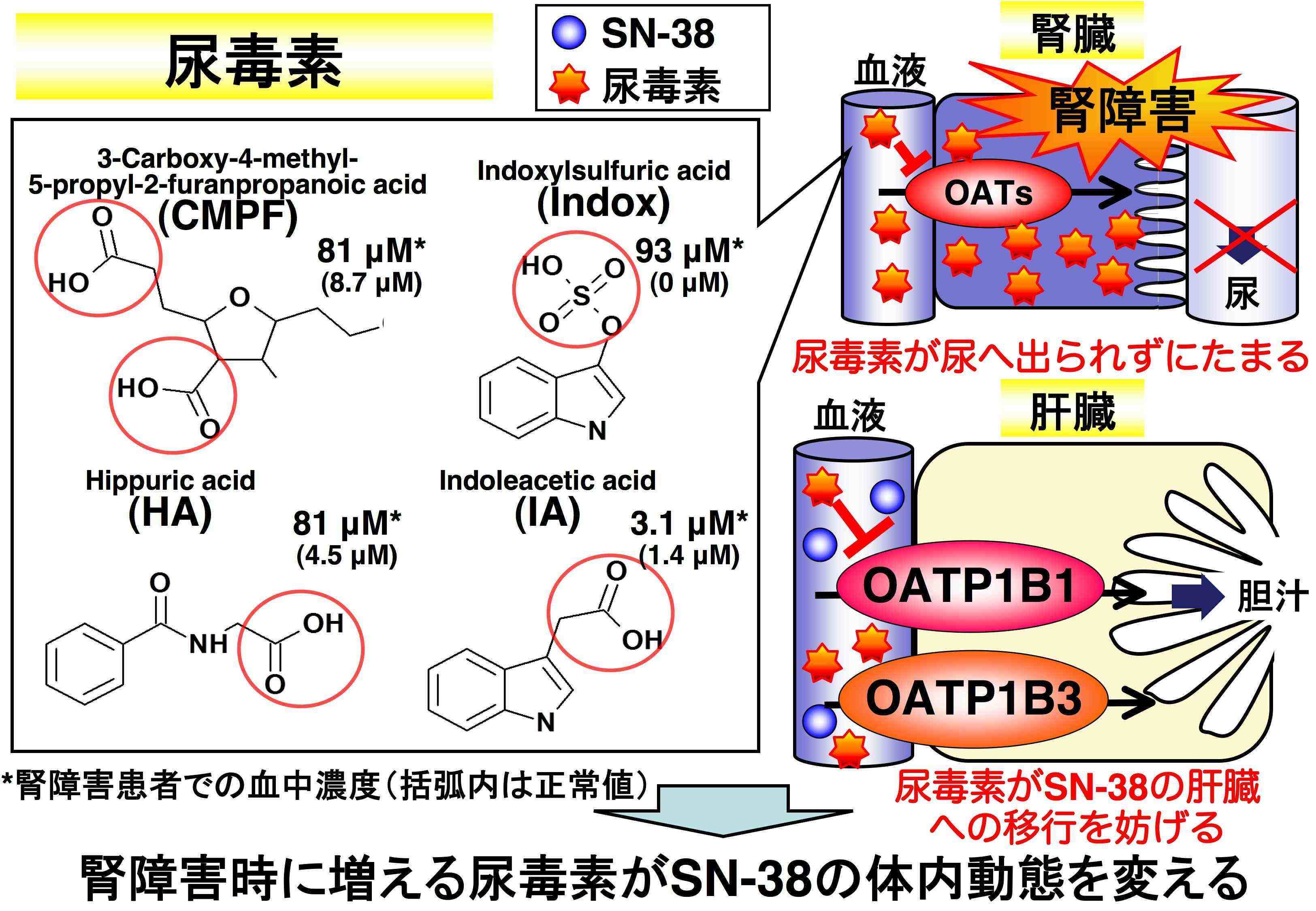
抗がん剤イリノテカン塩酸塩は、大腸がんや肺がんなどで広く使われています。イリノテカンによる抗がん作用は、その活性代謝物であるSN-38が発揮します(イリノテカンは体内でSN-38に変換され、抗がん作用を示すのです)。SN-38は肝臓でさらに代謝されたり胆汁中に排泄されたりして、体内から消失します。共同研究者である藤田健一博士らによる以前の研究で、イリノテカンを、腎障害を持つがん患者に投与したところ、このSN-38の血液中からの消失が著しく遅延し、一部の患者では骨髄抑制と呼ばれる副作用が見られました。腎障害は腎臓の機能が低下する病気ですので、一般に、腎臓で消失する薬物を投与する際には慎重である必要があります。しかし、SN-38は肝臓で消失する薬物ですので、それが血液中から消失しづらくなるこの研究成果は意外でした。一つの可能性として、腎障害時には尿毒素と呼ばれる物質が血液中にたまることが知られていますので、これがSN-38の肝臓への移行を妨げたことが考えられます。そこでこの論文では、その原因を探るため、ヒト肝細胞や、ヒト肝細胞に存在し薬物を細胞内へ取り込むトランスポーターOATP1B1やOATP1B3を導入した培養細胞を用い、SN-38の細胞内への取り込みに及ぼす尿毒素の影響を詳細に検討しました。さらに、腎障害患者から採取した血清がこれらトランスポーターにどのような影響を与えるかも調べました。その結果、SN-38の消失が遅延した原因には、①尿毒素の一部がSN-38の肝臓への取り込みに働くトランスポーターOATP1B1を直接妨げた(阻害した)ことと、②肝細胞でのOATP1B1自身の存在量(発現量)を低下させたこと、の少なくとも2つあることを見出しました。OATP1B1は多くの薬物の肝臓への取り込みに働いています。この知見は、イリノテカンのみならず多くの薬物を腎障害患者へ投与する際にも有益な情報になるものと考えられ、今後の薬物治療への応用が期待されます。
業績リストに戻る
トップページに戻る